暨南大学理工学院汪勇教授课题组硕士研究生李佳龙在Foods期刊(Q1, 影响因子5.2)发表了题为“The Anti-Inflammatory Mechanism of Flaxseed Linusorbs on Lipopolysaccharide-Induced RAW 264.7 Macrophages by Modulating TLR4/NF-κB/MAPK Pathway”的研究论文,由李颖与陈静副研究员共同指导,李颖副研究员为通讯作者。

一、研究背景
近年来,经研究证明,不平衡的饮食对慢性炎症疾病的影响很大。过度摄入宏量营养素会导致与代谢性疾病相关的炎症介质的持续激活,进而导致局部和全身的促炎标志物增加,最终发展为慢性炎症。慢性炎症性疾病很难确定和彻底根治,常用的非甾体类抗炎药物(NSAIDs)和糖皮质激素等药物又具有一定的副作用,如耐药性和依赖性等。因此,开发具有良好抗炎活性且不具有副作用的天然物质是未来发展策略。
亚麻籽是一种特殊的油籽,富含α-亚麻酸、木酚素和亚麻籽环肽等和多种生物活性物质。其中,亚麻籽环肽(FLs)约占亚麻籽和亚麻籽油的0.1%和0.3%,是一类独特的环状化合物。近年来,已发现天然食品源FLs在体内外具有多种生物活性,如抑制凋亡、抗癌和抗菌活性。此外,FLs具有显著的免疫抑制作用,可以降低成骨细胞生成、抑制THP-1巨噬细胞的激活并且对胃炎、肠炎和肝炎具有一定的缓解作用。因此,FLs具有作为膳食补充剂的潜力。然而,FLs的抗炎机制和其发挥主要功能的单体目前尚未阐明。本论文探究了FLs对LPS诱导的RAW 264.7巨噬细胞的抗炎机制,并鉴定了FLs在抗炎活性中靶向的受体蛋白。此外,通过分子对接预测了FLs主要活性单体,为促进具有显著抗炎活性的FLs单体作为功能活性成分在食品、药品和化妆品行业的应用奠定了科学基础。
二、研究方法
本研究首先用CCK8法测定了FLs对RAW 264.7巨噬细胞活力的影响,并且通过测定FLs对LPS诱导的RAW 264.7细胞所分泌的炎症标志性产物NO的影响,确定其对炎症的抑制作用。用Western Blot(WB)、RT-qPCR以及ELISA法检测FLs对炎症因子以及炎症介质在蛋白与基因水平的抑制作用。进一步用WB和免疫荧光法探究FLs发挥抗炎作用的机制。此外,通过结合分子模拟对接与HPLC结果,并通过NO抑制实验确定主要发挥抗炎作用的FLs单体。
三、研究结果
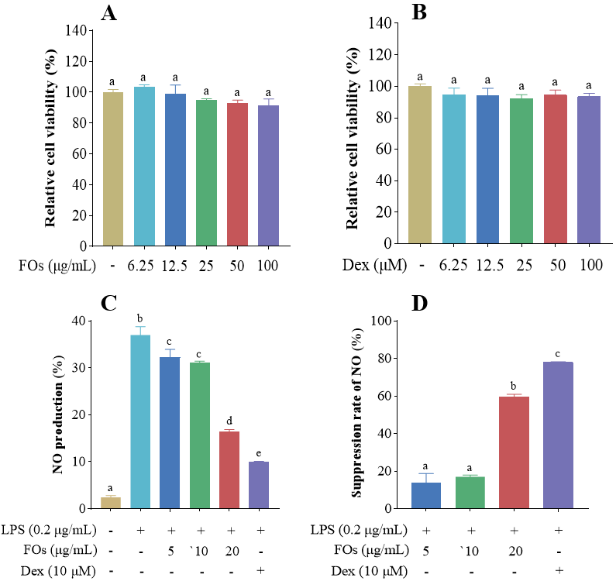
FLs在0-100 μg/mL的浓度下,对细胞活性的影响无显著性差异。FOs通过以剂量依赖方式抑制NO的产生,并且在20 μg/mL时对NO的产生有较好的抑制作用。以上结果提示FLs对RAW 264.7巨噬细胞无明显毒性,并且对炎症有明显的抑制作用。
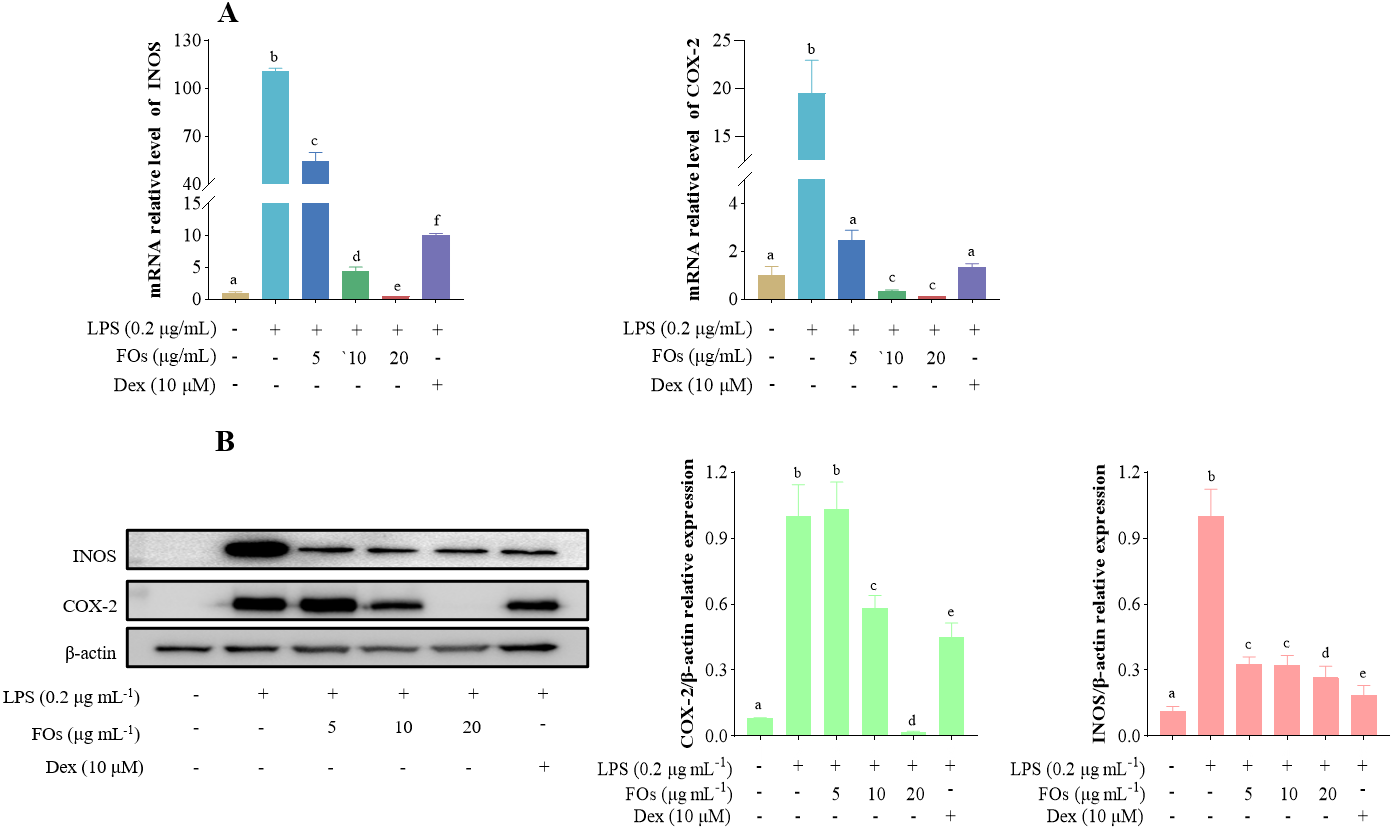
FOs通过以剂量依赖方式在基因与蛋白水平抑制炎症介质iNos与COX-2的产生。在10 μg/mL时已有较好的抑制作用,并且在20 μg/mL时与阳性药物地塞米松(Dex)的作用效果相近。以上结果提示FLs能通过抑制炎症介质的转录与表达发挥抗炎活性。
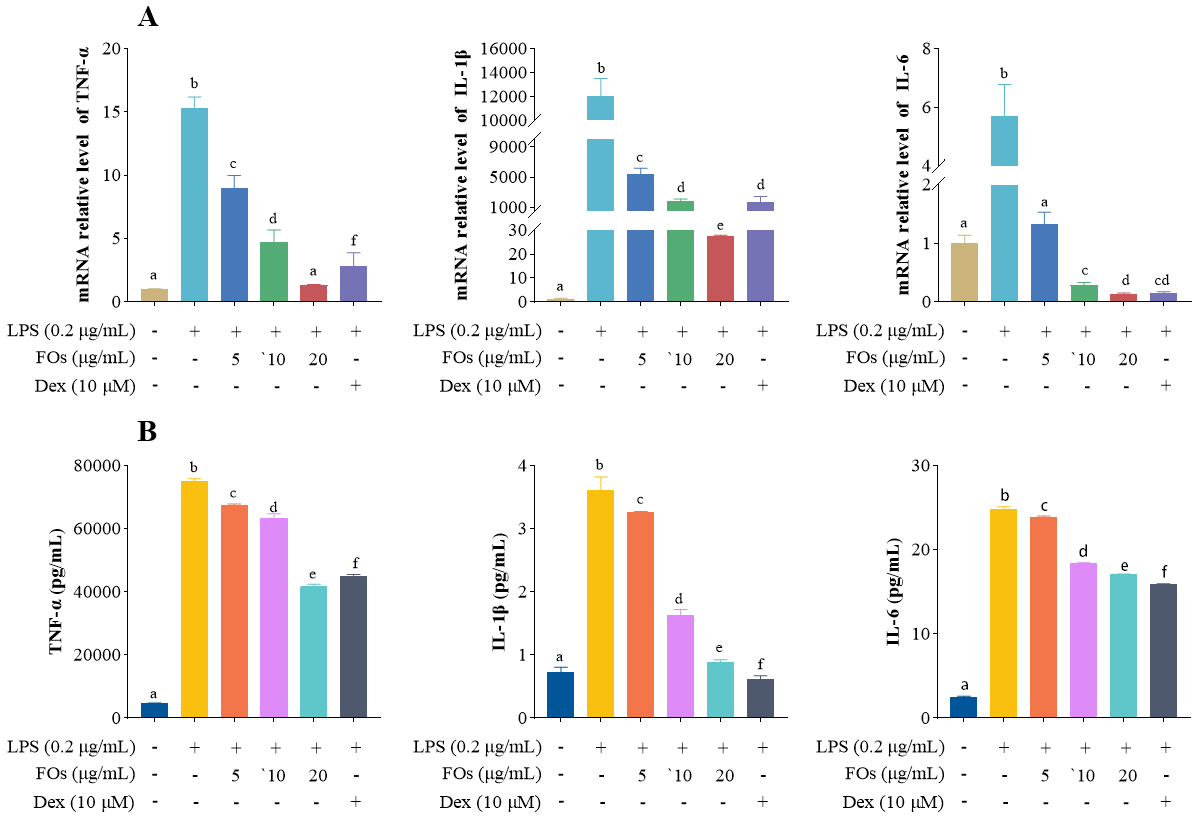
FLs通过以剂量依赖方式抑制三种标志炎症因子的转录与表达。在10 μg/mL时对TNF-α, IL-1β和IL-6的蛋白与基因转录有较好的抑制作用,并且在20 μg/mL时与Dex的作用效果相近。以上结果提示FLs能通过抑制炎症因子的转录与表达发挥抗炎活性。
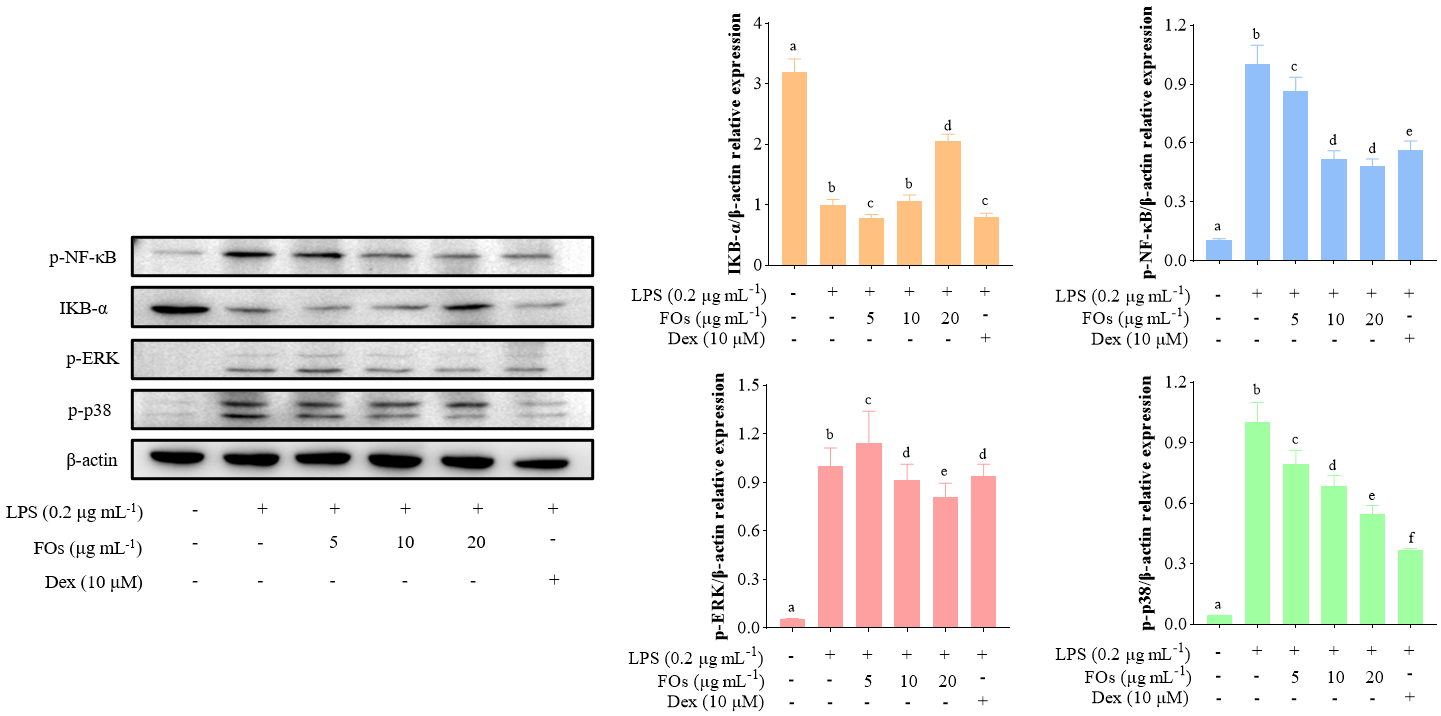
FLs能以剂量依赖性方式提高IκB-α蛋白的表达水平,并以剂量依赖性方式抑制p-NF-κB、p-P38和p-ERK的表达。以上结果提示FLs能通过调节NF-κB与MAPK信号同路中关键信号蛋白的表达发挥抗炎活性。
FLs可通过以剂量依赖方式抑制NF-κB的磷酸化与p-NF-κB核转位从而抑制炎症反应。
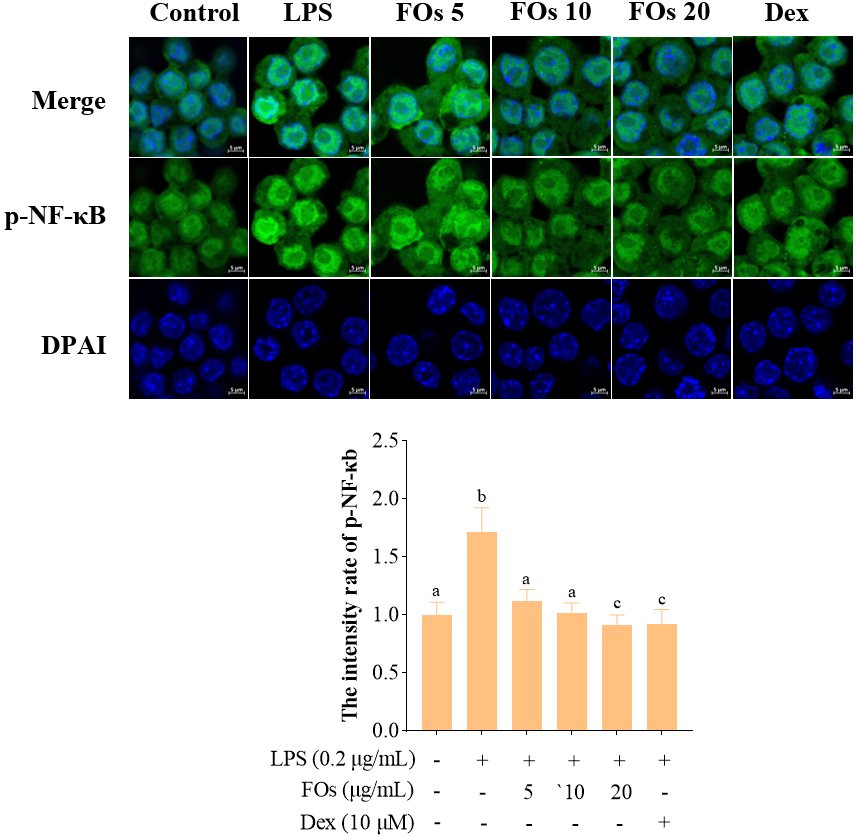
FLs可通过以时间依赖方式抑制炎症关键膜受体蛋白TLR4与NF-κB信号通路IκB-α蛋白的表达从而抑制炎症反应。
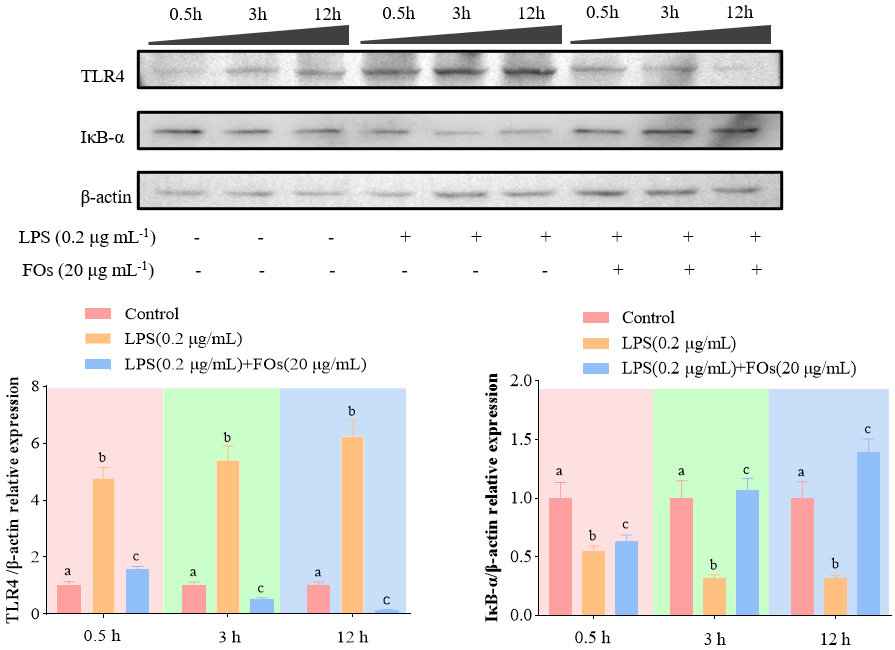
分子模拟对接结果显示,8个FLs单体与TLR4之间的配体-蛋白质相互作用力极强,与TLR4有着较好的口袋对接的适应力。
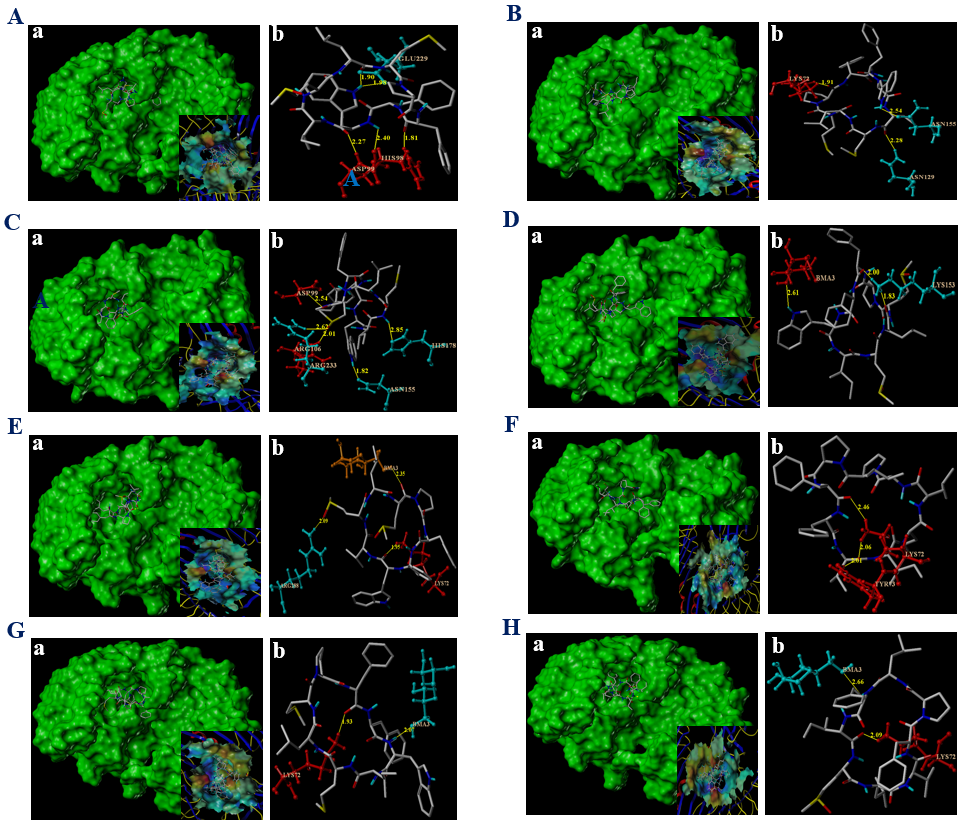
进一步分离并探究含量多且与TLR4蛋白作用力强的FLs单体FLA与FLE的抗炎活性。FLA与FLE对RAW 264.7巨噬细胞的活力无明显影响,且均通过以剂量依赖方式抑制NO的产生。此外,与分子对接结果一致的是,FLE对炎症的抑制效果要强于FLA。
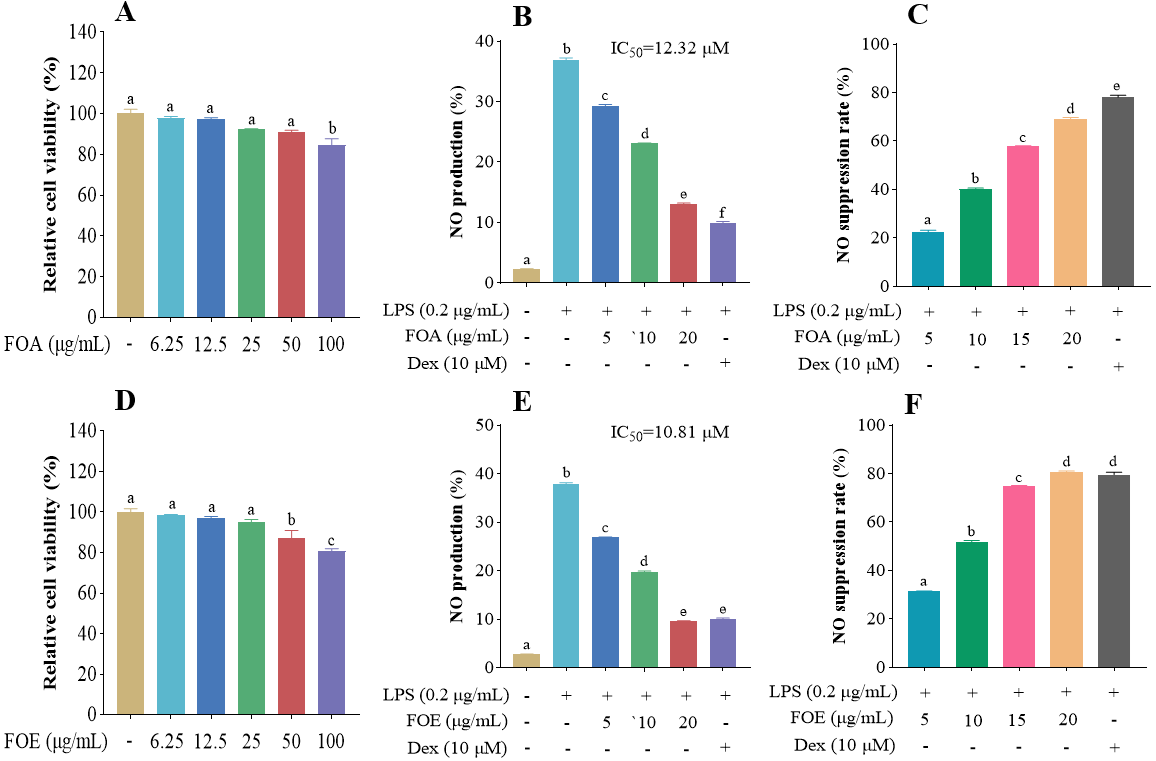
四、研究结论
本研究揭示了FLs对LPS诱导的RAW 264.7巨噬细胞炎症反应的靶向抑制效应。FLs可抑制NF-κB/MAPK信号通路传导,从而降低促炎因子的分泌和促炎介质的表达。此外,FLs还通过靶向TLR4受体蛋白表达发挥显著的抗炎活性。通过计算机模拟分析显示,FLs单体与炎症靶标蛋白TLR4之间存在结合作用,根据HPLC结果确定亚麻环肽A和E为主要的抗炎单体。因此,FLs具有成为天然抗炎膳食补充剂的潜力。未来将进一步研究FLs单体与其体内外抗炎活性的构效和量效关系,并探索不同FLs单体的绿色高效规模化制备方法。
本研究工作得到了国家重点研究发展计划(2018YFE0108400)和国家自然科学基金(32072252、21319089)的支持。
作者简介:

李颖,法国博士,长期从事生物质资源高值化综合利用技术研发与应用研究,重点研究天然产物绿色萃取关键技术和机理,及其在功能食品、化妆品、饮料、饲料配料等大健康领域的产业化应用。2015年将“绿色萃取”理念和技术首次引入国内应用于特色生物质资源开发,曾任国家高新技术龙头企业部门技术总监,现任暨南大学食品科学与工程副研究员/副系主任(主持工作),广东省食品学会理事/副秘书长,广东省“扬帆计划”第一核心成员。以第一完成人主持/核心参与国家自然科学基金项目、国家重点研发项目课题任务等项目共7项。累计发表高水平论文30余篇,其中第一或通讯作者SCI论文20篇(A1类17篇);主编Springer英文著作2部《Plant Based “Green Chemistry 2.0”》和《Essential Oils as Reagents for Green Chemistry》,参编英文著作3部共4章节。此外,以口头报告形式参加国内外会议二十余次,入选2018年第三届“天然产物绿色萃取”国际会议和第二届“迷迭香及其益处”国际会议组委会;担任SCI期刊Green Chemistry, ACS Sustainable Chemistry & Engineering, Food Chemistry和LWT等期刊审稿人。2014年获欧洲超声波化学协会颁发的“优秀青年科学家”奖,2015-2016年分别入选昆明市人社厅“三五工程”和云南省组织部“百人计划”人才,2020年入选“暨南双百英才计划”暨南杰青(第一层次)。

李佳龙,暨南大学硕士研究生,高级健康管理师。研究方向为天然活性产物的开发与应用。主要探索天然生物活性物对各类炎症性疾病的影响,可以开展多种体内、外生物实验,并且熟练掌握生物实验及生物信息技能,目前在Foods、Food Bioscience等国际期刊杂志上发表SCI论文4篇,申请发明专利1项,参编科普著作1部。


